ما أهم أعمال الفيزياء النووية التي أدت إلى اكتشاف النيوترون
ملاحظة هامة : يحتوي هذا الموقع على أكثر من 600 كتاب فيزياء يمكن الوصول إليها من صفحة : كتب الفيزياء
ــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
لقد كان اكتشاف النيوترون عمليًّا تتويجًا لمرحلة بحث طويلة ولأعمال مهمة في الفيزياء النووية استمرت لأكثر من ربع قرن من الزمان. وعلينا أن نتذكر دائمًا أنه قلما تتكشف الحقائق العلمية في صورتها النهائية مرة واحدة.
في عام 1896، اكتشف الفيزيائي الفرنسي أنطوان هنري بكريل (1852–1908) ظاهرة جديدة وهي أن أملاح عنصر اليورانيوم تصدر أشعة نافذة تؤثر على الألواح الفوتوغرافية وتتأثر بالمجالات الكهربية والمغناطيسية. سُميت هذه الظاهرة بالنشاط الإشعاعي.
يُعرف النشاط الإشعاعي (الشدة الإشعاعية Radioactivity) بأنه عملية التفكك التلقائي للنواة النشطة (غير المستقرة)، ويصاحب هذه العملية انبعاث إشعاعات من جسيمات ألفا أو بيتا أو أشعة كهرومغناطيسية. ويُستخدم مفهوم النشاط الإشعاعي للتعبير عن عدد الأنوية المُشعة التي تتحلل في الثانية الواحدة.
بعد ذلك وفي العام 1898 اكتشفت ماري كوري عناصر مشعة جديدة أطلقت عليها أسماء البولونيوم (نسبة إلى وطن مولدها) والراديوم (نظرًا لشدة نشاطه الإشعاعي)، حيث قامت بمساعدة زوجها بيير كوري بفصل الراديوم والبولونيوم من خام البتشبلند pitchblende؛ وهو خام لونه بني يميل إلى السواد، وله بريق مميز ويحتوي أساسًا على أكسيد اليورانيوم وهو المصدر الرئيسي لخام اليورانيوم، لكنه يحتوي أيضًا على عناصر أخرى ذات نشاط إشعاعي.
إن اكتشاف النشاط الإشعاعي قد سجل بداية عصر جديد في الفيزياء. وحطمت هذه الاكتشافات الاعتقاد الثابت والمتوارث بأن العناصر لا تتحول، وأن ذرة العنصر لا تتفكك.
وفي عام 1898، قام الإنجليزي رزرفورد بدراسة خواص الأشعة الناتجة عن اليورانيوم، وسجل وجود أشعة لينة (ذات قدرة محدودة على اختراق المواد أطلق عليها اسم «ألفا α» الحرف الأول في اللغة اليونانية) ووجود أشعة قاسية (أكثر قدرة من أشعة ألفا على اختراق المواد أطلق عليها اسم «بيتا β» الحرف الثاني في اللغة اليونانية). وفي عام 1900 اكتشف بول فيلارد النوع الثالث من الأشعة، وأُطلق عليها اسم «جاما γ» الحرف الثالث في اللغة اليونانية، وهذه الأشعة أقدر من سابقتيها في القدرة على اختراق المواد.
يتضح من ذلك أنه مع بدايات القرن الماضي لم يكن لدى الفيزيائيين، في ذلك الوقت، لإجراء التفاعلات النووية سوى جسيمات ألفا الناتجة عن تفكك البولونيوم الذي اكتشفته ماري كوري، والتي كانت بكرمها وتعاونها تمنحه لزملائها لإجراء تجاربهم.
ويمكننا اعتبار رزرفورد هو مؤسس (أبو) علم الفيزياء النووية، حيث إنه:
- في عام 1908 أثبت أن جسيمات ألفا التي انبعثت من نواة اليورانيوم عبارة عن نواة ذرة الهليوم.
- وفي عام 1911 أدخل مفهوم نواة الذرة نتيجة تشتت جسيمات ألفا على رقيقة من الذهب.
- وفي عام 1917 بين رزرفورد أنه يمكن إجراء تحول صناعي للعناصر، حيث حصل على الأكسجين والهيدروجين من النتروجين باستخدام جسيمات ألفا طبقًا للتفاعل 7N14(α, p) 8O17
- وفي عام 1919 عثر رزرفورد على أول دليل وبرهان على وجود البروتون في النواة.
جذب انتباه ماكس بلانك عمليات الإشعاع من الأجسام الساخنة. كانت النتائج التي حصل عليها على اختلاف بَيّنْ وواضح مع توقعات الديناميكا الحرارية وبالتالي الفيزياء التقليدية، إذ وجد أن الطاقة المنبعثة محددة وليست متصلة، على الرغم من أن الطاقة الممتصة في الجسم طاقة متصلة.
استطاع بلانك الحصول على علاقة تربط بين طاقة وتردد الإشعاع المنبعث. ونشر عام 1900 اشتقاقه لهذه العلاقة التي كانت على أساس فكرة جديدة هي أن الأشعة المنبعثة من المصدر تخرج على هيئة حزم وتأخذ فقط قيمًا محددة، أسماها كوانتا عن اللاتينية «كم»؟ والثابت h في هذه العلاقة يسمى حاليًا ثابت بلانك ويساوي 6.625 ×10-27 ارج ثانية. وبيّن أن هذه الأشعة لها طبيعة كهرومغناطيسة.
طبقًا لافتراض بلانك، كل الأشعة الكهرومغناطيسية «عبارة عن كم من الطاقة»، وتحدث كحزمة (ربطة واحدة) محددة يطلق عليها اسم فوتون.
«كم» طاقة الفوتون = حاصل ضرب ثابت بلانك في التردد.
كانت فكرة ماكس بلانك الجديدة عن الكوانتا غريبة، لكن النتائج كانت تتوافق مع الظواهر. هذا العمل لم يكن فقط أهم أعمال بلانك، لكنه أيضًا العمل الذي يُعتبر نقطة بداية التحول في تاريخ الفيزياء. في البداية لم تظهر أهمية هذا الاكتشاف وتأثيره على الفيزياء الكلاسيكية (التقليدية)، وتدريجيًّا أصبح هذا الاكتشاف رائعًا كلما أعطت تطبيقاته توافقًا مع الظواهر التي كانت تتعارض مع النظرية التقليدية.
بداية مولد الفيزياء الحديثة
إن أحد أهم هذه التطبيقات المُطورة لهذه الفكرة استخدمها اينشتاين في شرح ظاهرة التأثير الكهروضوئي. وطبقها بوهر على نموذج رزرفورد للذرة. لقد شكل العلماء، من أمثال اينشتاين وبور وهايزنبرج، الفيزياء الحديثة باستخدام الفكرة الجديدة الرائعة لماكس بلانك وصفة «الكم» الجديدة للطاقة (وهنا يمكن أن نعتبر بداية مولد الفيزياء الحديثة). ويعتبر ثابت بلانك أحد الثوابت الأساسية في الكون.
في الواقع لم يكن بلانك نفسه متأكدًا من أن فكرته والثابت الذي حصل عليه ما هو إلا حل رياضي لمسألته. والذي أصبح أحد الثوابت الجوهرية والأساسية في الفيزياء.
في عام 1913 أدخل نلز بور نظرية الكم في مدارات الذرة شبه نموذج تركيب الذرة بالنموذج الكواكبي بدلاً من نموذج تومسون الذي شبه فيه الذرة بكعكة الزبيب، كما بين أن النشاط الإشعاعي خاصية نووية. وأيضًا بيّن فردريك سودي العلاقة بين العدد الذري وشحنة النواة، كما أدخل مصطلح النظير.
كانت الرغبة في معرفة مكونات النواة تتطلب إجراء تفاعلات نووية وكانت هذه التفاعلات تجرى باستخدام الوسائل المتاحة حتى نهاية فترة العشرينيات من القرن العشرين، وهي العناصر التي تشع تلقائيًّا جسيمات ألفا مثل البولونيوم والراديوم التي اكتشفتها السيدة ماري كوري. تطلبت تلك الرغبة في معرفة كنه الذرة ومكوناتها الحاجة إلى مصدر أقوى يمدنا بمقذوفات ذات كثافة أعلى وطاقة أكبر. ولقد لبت الاختراعات تلك الحاجة فيما يسمى بالمسرعات (المعجلات) ولاحقًا في المفاعلات النووية.
النظائر المشعة
أدت الدراسات التي أجرتها ماري كوري ورزرفورد وآخرون إلى أنه يوجد في الطبيعة حوالي 30 عنصرًا لها خاصية النشاط الإشعاعي الطبيعي، لكن اختراع المسرعات أتاح إمكانية الحصول على العديد من النظائر المشعة، فيما يسمى النشاط الإشعاعي الصناعي.
حصل كل من فردريك جوليو وزوجته إيرين جوليو كوري (بنت بيير وماري كوري) على جائزة نوبل في الكيمياء عام 1935 اعترافا بحصولهما على مواد إشعاعية جديدة. جدير بالذكر أنه كانت لهما مساهمات أساسية في اكتشاف النيوترون، سنتحدث عنها لاحقًا.
كانت أبحاث شادويك (أحد تلامذة رزرفورد) الخاصة تركز على النشاط الإشعاعي. وكما عرفنا أن رزرفورد كان قد اكتشف البروتون، داخل نواة الذرة في عام 1919، لكنه كان يعتقد، وكذلك غيره من الباحثين، أن البروتون فيما يبدو ليس المكون الوحيد لجسم النواة.
ولما كانت دراساتهم في تفكك واضمحلال الذرات، فقد كانوا يلاحظون باستمرار أن العدد الذري أقل من الكتلة الذرية. فعلى سبيل المثال، ذرة الهيليوم لها كتلة ذرية من 4، ولكن العدد الذري (الشحنة الموجبة)، وحيث إن الإلكترونات لا كتلة لها تقريبًا لذلك يبدو واضحًا أن شيئا ما يوجد إلى جانب البروتونات في النواة.
كان أحد التفسيرات الرائدة في هذا الصدد أنه توجد بروتونات وإلكترونات إضافية في النواة، البروتونات تساهم بكتلتها ويتم إلغاء شحناتها الموجبة بواسطة شحنات الإلكترونات السالبة. ففي مثال الهليوم، ستتكون النواة من أربع بروتونات وإلكترونين لإنتاج كتلة 4 ولكن بمحصلة شحنة 2 فقط. كما أشار رزرفورد أيضًا إلى فكرة وجود جسيم له كتلة وليس له شحنة أطلق عليه اسم النيوترون. وقد كان تخيله أنه عبارة عن بروتون يلتصق (يقترن) به إلكترون. ولم يكن هناك أي دليل على صحة أي من هذه الأفكار.
وبينما كان جيمس تشادويك يعمل على أمور أخرى، احتفظ في عقله الباطن بتلك المشكلة. لقد أمضى ما يقرب من عقد من الزمان ليبحث عن هذا الجسيم المراوغ المتعادل الشحنة.
جسيمات جديدة في الذرّة
وحتى عام 1930، كان يفترض أن الجسيمات الأساسية في الذرّة هي البروتونات والإلكترونات فقط. وفي ذلك الوقت ظهر مبدأ عدم اليقين، ومن حسابات «حبس الجسيمات في صندوق «from «particle-in-a-box» type confinement calculations، تبين أنه لا يوجد ما يكفي من الطاقة المتاحة (الطاقة اللازمة لاحتجاز إلكترون في نواة ذات بعد 5 فيرمي تقدر بـحوالي 250 مليون إلكترون فولت) لاحتواء الإلكترونات في النواة؛ حيث يمكن حساب الطاقة اللازمة (تقريبًا) لحبس واحتجاز جسم في حدود بعد معين باستخدام الطول الموجي لـ «دي برولي» مساويًا لذلك البعد. وبهذا بدا واضحًا أنه لا توجد إلكترونات في داخل النواة.
اشتعل النشاط في أوربا للبحث عن هذا الجسيم المراوغ الملقب بالنيوترون للتعرف عليه ودراسة خصائصه، حتى ظهرت بوادر الحل في ألمانيا عام 1931. بينت ملاحظات بيكر مع بوثه أن الأشعة المنبعثة عند تصادم جسيمات ألفا مع أهداف من البريليوم، والبورون، أو الليثيوم، تكون لها قدرة نفاذ عالية، وبينت الملاحظات أيضًا أن الأشعة التي تصدر عن البورون تكون أقدر على النفاذ من تلك الصادرة عن البريليوم. تتفق هذه النتائج مع الافتراض الذي يأسر جسيمات ألفا داخل البريليوم (أو البورون) مع انطلاق كمية الطاقة الزائدة على هيئة «كم» إشعاعي. وللأسف لم تسجل أي ملاحظات غير عادية عن خواص هذه الأشعة، وربما يرجع ذلك لعدم مناسبة تنظيم التجربة من ناحية ولضعف إشعاعية المصدر المستخدم للحصول على جسيمات ألفا من ناحية أخرى.
على الجانب الآخر في فرنسا، لاحظت إيرين كوري وزوجها فردريك (1932) أن هذه الأشعة الصادرة عن البريليوم أو البورون لها المقدرة على طرد البروتونات بسرعة ذات قيمة (طاقة قدرها 5.3 ملايين إلكترون فولت) من المواد الهيدروجينية. وتلاحظ أنه عندما كان يوضع الشمع أو أي مادة هيدروجينية أخرى في طريق مسار هذه الأشعة، كانت تتزايد درجة التأين في غرفة التأين لدرجة التضاعف، أحيانًا.
فسر الباحثون نتائج هذه التجارب على أن هذه الأشعة المتعادلة (جاما افتراضًا) تقوم بطرد البروتونات من المواد الهيدروجينية مثلما تقوم الفوتونات بطرد الإلكترونات في ظاهرة التأثير الكهروضوئي.
نال اينشتاين جائزة نوبل في الفيزياء عام 1921 لخدماته في الفيزياء النظرية واكتشاف قانون التأثير الكهروضوئي. وعندما أعلنت هذه النتائج قال رزرفورد «أنا لا أصدق ذلك»، وقال آخر «كم هم من أغبياء؟!! لقد وجد البروتون المتعادل دون معرفة».
وبإجراء مزيد من التجارب للتعرف على خصائص هذه الأشعة، بيّن شادويك أنها لا تطرد فقط البروتونات من المواد الهيدروجينية، لكنها تطردها أيضًا من أي عناصر خفيفة أخرى، وأن هذه الأشعة أقوى في الاتجاه الأمامي من الاتجاه العكسي. ولأن الضوء لابد أن يشع في جميع الاتجاهات، فقد أوحى ذلك بأن هذه الأشعة على الأرجح جسيمات وليست ضوءًا، كما أنه يلزم طاقة كبيرة جدًا لتقوم أشعة جاما بطرد بروتون من النواة، طاقة أكبر بكثير من مقدار الطاقة الناتجة عن قذف البريليوم بجسيمات ألفا. لذا كان من الصعب تفسير هذه النتائج على أساس التماثل مع حالة التأثير الكهروضوئي.
كيف تجد الأعمى وسط الميدان؟!
ثار التساؤل كيف تجد الرجل الأعمى وسط ميدان عام مزدحم بالبشر؟ والإجابة المنطقية السهلة هي عن طريق الناس الذين يصطدم بهم وردود أفعال الذين يدفعهم جانبًا. استخدم شادويك هذه الأشعة ليركل بها ذرات النتروجين والهيدروجين، وبمقارنة الارتداد قام بحساب الكتلة فوجد أنها مساوية لكتلة البروتون تقريبًا، وعلى هذا الأساس وتلك النتيجة يمكن أن تختفي مشكلات حسابات التصادمات من ناحية الترددات وانتقال الطاقة بين الكتل، (نجح شادويك في تجاربه وأثبت أن كتلة هذا الجسيم تزيد بمقدار 0.1 في المائة عن البروتون أي حوالي 1.29 MeV). إنه الجسيم الذي لا شحنة له، الجسيم الذي سبق أن أسماه رزرفورد النيوترون في عام 1920. ذلك الجسيم الذي يتكون من بروتون وإلكترون في ارتباط لصيق.
كان لفكرة الارتباط اللصيق ووجود إلكترونات داخل النواة مشكلات إذ كان يجب التخلي عن بعض خصائص الإلكترون التي ترتبط به وهو خارج النواة مثل اللف المغزلي والعزم المغناطيسي، بالإضافة إلى مشكلة حبسه في داخل النواة. وسرعان ما تقبل هايزنبرج هذا الاكتشاف وأثبت أن هذا الجسيم (النيوترون) قائم بذاته ولا يتكون من بروتون وإلكترون لصيق, وأنه بذلك يصبح المكون الثاني في النواة والثالث في الذرة، إنه النيوترون وإنه أيضًا من الأشعة المؤينة؛ وبهذا تغير مفهومنا عن التركيب الذري مرة أخرى.
تم قبول نتائج شادويك بسرعة، وأن النيوترون جسيم قائم بذاته، حيث تم استبعاد فكرة وجود إلكترونات حرة في النواة أو حتى لصيقة ومقترنة بالبروتونات. ويبين الشكل التالي التجربة التي أجراها شادويك لاكتشاف النيوترون.
وقد تم تفسير التجارب على النحو التالي:
عندما تصطدم جسيمات ألفا الناتجة عن مصدر مشع مع نواة البريليوم تحولها إلى نواة الكربون، ويسفر ذلك عن إطلاق نيوترون حر. عندما يصطدم هذا النيوترون بنواة الهيدروجين الموجودة في الشمع، فإنه قد يحرر بروتونا.
على الجانب الآخر، فإن حقيقة وجود عزم مغناطيسي للنيوترون تستوجب اقتراح أن يكون للنيوترون تكوين داخليّ من الشحنات بالرغم من كونه ككل متعادل الشحنة. جسيمات أصغر تسمى كواركات لها شحنات موجبة وسالبة.
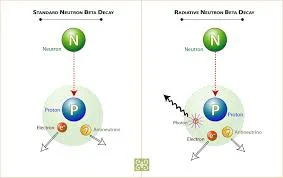
والنيوترون في النواة مستقر، لكن عمر النصف للنيوترون الحر حوالي 12 دقيقة ويتحول النيوترون إلى بروتون وإلكترون والمضاد للنيوترينو. إن عملية تفكك النيوترون أدت إلى اكتشاف مضاد النيوترينو. وتفسر هذه العملية على أنها تحول داخلي في الكواركات من نوع إلى آخر. وتبعًا لنظرية الكم، فالنيوترون كأي جسيم ذري آخر له خاصية الموجه، ويهتم مجال بصريات النيوترونات بدراسة مواضيع مثل حيود واستقطاب أشعة النيوترونات.
أجريت العديد من الدراسات لمعرفة خواص هذا المولود الجديد، فلقد عينت كتلته وحجمه ولفه المغزلي وعمر النصف للنيوترون الحر.
بناء على اكتشاف النيوترون واعتباره حقيقة مسلما بها، فباستثناء الهيدروجين، تتكون نوى الذرات من البروتونات والنيوترونات، والتي بالتالي يشار إليها مجتمعة بـ «النيوكليون». هذه الأفكار الجديدة والاكتشافات المتسارعة غيرت بشكل كبير من صورة الذرة، وسرعان ما وجد علماء الفيزياء النووية في النيوترون قذيفة مثالية «رصاصة» لقصف النوى الأخرى. على عكس الجسيمات ذات الشحنة، التي تلقي مقاومة تنافر من الدفاعات الكهربية في النواة. هذا الجسيم الجديد المتعادل الشحنة يمكنه أن يسبر أغوار النواة بل يمكنه أن يستقر في نواة عنصر الهدف ليحولها إلى نظير أو لعنصر أثقل وأكبر كتلة.
أهم تفاعلات النيوترون مع المادة:
1- التصادم المرن:
في هذه الحالة يسقط النيوترون على النواة بحيث يعطيها جزءا من طاقته ويتشتت هو بطاقة أقل من طاقته الإبتدائية بينما ترتد النواة بطاقة تساوي تلك المنتقلة إليها بالتصادم.. ويسمى هذا التصادم بالمرن لأن كمية وطاقة الحركة محفوظتين قبل وبعد التصادم.
قد يتم التصادم المرن بصورتين :
أ- قد يحدث امتصاص أولا للنيوترون بواسطة النواة المقذوفة ويتم تكوين ما يعرف بالنواة المركبة التي تقوم بإطلاق نيوترون آخر بعد ذلك وهو النيوترون المتشتت.
ب_ قد يحدث التفاعل مباشرة دون المرور بمرحلة النواة المركبة حيث يتشتت النيوترون مباشرة عن النواة.
2- التصادم اللامرن:
وفيه لا تكون طاقة الحركة محفوظة إذ أنه عند سقوط النيوترون على النواة فإنه يعطيها جزءا من طاقته يستخدم لإثارتها أولا ثم تمتص جزءا آخر لتنطلق به بطاقة حركة معينة .
3- تفاعلات الأسر:
حيث تقوم النواة بإسر النيوترون الساقط عليها وامتصاص كل طاقته فتصبح لأجل ذلك في حالة إثارة.. بإعتقادكم كيف يمكن لنواة كهذه أن تعود لوضع الإستقرار؟؟
ومن الجدير بالذكر أن مثل هذه التفاعلات تتمتع باحتمال تفاعل كبير ومن ثم يمكن استخدامها للكشف عن النيوترونات بكفاءة..
4- الإنشطار النووي:
عندما تمتص بعض الأنوية النيوترونات فإن طاقة الإثارة تصبح كافية لإحداث الإنشطار النووي وقد وجد أن ذلك يحدث للأنوية الثقيلة وبخاصة اليورانيوم وما بعده حيث تنشطر النواة عند قذفها بنيوترون إلى نواتين أصغر منها تعرفان بشظيتي الإنشطار وتنطلق من هذا التفاعل طاقة هائلة تقدر ب 200 م أ ف ,,
5- تفاعل النيوترونات السريعة:
تتفاعل النيوترونات السريعة مع المادة حيث تمتص بواستطها وينتج عن ذلك جسيمات مشحونة كالبروتون..
أما النيوترونات السريعة جدا ذات الطاقة الأكبرمن 100 م أ ف فإنه ينتج عن تفاعلها مع المادة فيضا من الفوتونات أو الجسيمات الخفيفة ةالتي تضم العديد من إحتمالات التفاعل .
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
سجل إعجابك وشارك زملاءك من الزر أدناه لتصلكم مواضيعنا القادمة إن شاء الله تعالي